Varroa destructor ¿El “Caballo de Troya”? El vector silencioso que potencia la diseminación de los virus en la apicultura argentina.
SALINA Marcos Daniel, REYNALDI Francisco José.
Centro de Microbiología Básica y Aplicada -CEMIBA-, Facultad de Ciencias Veterinarias, Universidad Nacional de La Plata; Consejo Nacional de Investigaciones Científicas y Técnicas, CCT-La Plata
Introducción
La apicultura argentina enfrenta importantes desafíos, tales como la fluctuación del precio internacional de la miel, la competencia de países con menores costos de producción y las dificultades para acceder a mercados diferenciados afectan la rentabilidad del productor. Como mencionamos en “Los virus que afectan a las Abejas. ¿Un problema invisible? (1ra parte)”, existen varios factores que inciden en las pérdidas de colmenas entre los que se destacan los problemas sanitarios, la falta de alimento natural en ciertos períodos y el estrés ambiental. Dentro de los problemas sanitarios, Varroa destructor es el enemigo más importante y extendido en la apicultura mundial. Este ácaro parasita tanto a las abejas adultas como a las crías, alimentándose de sus cuerpos grasos y debilitando su sistema inmunológico. Para complejizar este escenario, Varroa destructor no solo produce daño directo, sino que también actúa como vector de virus (un verdadero Caballo de Troya) que agravan el cuadro sanitario. En particular los virus se multiplican con mayor facilidad en colonias infestadas, generando abejas malformadas, o con comportamientos anormales y hasta la muerte..
Virus que afectan las Abejas en Argentina
A nivel Mundial se han detectado más de 70 virus en muestras de abejas melíferas, 10 de estos virus se reportaron en Argentina hasta el momento (Salina y col., 2021). Dentro de este repertorio viral, 5 agentes virales han demostrado ser de particular importancia debido a su alta prevalencia o al severo impacto que provocan en las colonias: el Virus de las Alas Deformadas (DWV), el Virus de la Cría Ensacada (SBV), el Virus de las Celdas Reales Negras (BQCV), el Virus de la Parálisis Crónica de las Abejas (CBPV) y el denominado “Complejo AIK”, conformado por el Virus de la Parálisis Aguda (ABPV), el Virus de la Parálisis Aguda Israelí (IAPV) y el Virus de Cachemira (KBV), que se caracterizan por compartir manifestar sintomatología similar en abejas adultas.
En Argentina, los principales virus que afectan a las abejas melíferas pertenecen a las familias Iflaviridae y Dicistroviridae, destacándose el virus de las alas deformadas (DWV), el virus de la cría ensacada (SBV), el virus de la parálisis aguda israelí (IAPV), el virus de la parálisis aguda (ABPV) y el virus de la cría negra (BQCV). En los últimos años DWV resulta ser el virus más prevalente, ampliamente distribuido en todas las regiones del país. SBV y BQCV también se detectan de forma recurrente en diversas áreas productivas, aunque con prevalencias generalmente menores. En tanto, los virus IAPV y ABPV, pertenecientes al complejo de parálisis aguda (AIK), presentan una distribución más heterogénea, pero su circulación se ha confirmado en distintas zonas del país durante los últimos años.
En conjunto, estos virus muestran una amplia dispersión geográfica y temporal en la apicultura argentina. Su presencia, frecuentemente subclínica, puede intensificarse ante factores de estrés o desequilibrios sanitarios, especialmente en colonias debilitadas o con alta carga de Varroa destructor, actuando este ácaro como amplificador clave en la dinámica viral y contribuyendo al deterioro general y pérdidas de colmenas.
Virus de las Alas deformadas
El virus de las alas deformadas, DWV por sus siglas en inglés, es considerado el agente viral más perjudicial para la apicultura a nivel global y a consecuencia el patógeno más intensamente estudiado. Aislado por primera vez de abejas con alas deformes en Japón 1982, y desde entonces ha sido detectado asociado a perdidas de colmenas en todo el mundo. En Argentina, en el año 2010 nuestro grupo de trabajo reportó por primera vez su presencia en muestras de la provincia de Buenos Aires (Reynaldi y col., 2020).
Este virus ingresa a las colmenas principalmente mediante el ácaro Varroa destructor, que inocula el virus directamente en la hemolinfa de las abejas durante su alimentación. Además, puede transmitirse de forma horizontal entre abejas por contacto, trofalaxia o cuidado de cría, y también de forma vertical desde la reina hacia la descendencia o durante la cópula con zánganos infectados, perpetuando la infección una vez dentro de la colonia. Otros mecanismos importantes son la deriva de vuelo, el pillaje de colmenas debilitadas y la introducción accidental de abejas, cuadros o reinas infectadas, lo que explica la rápida expansión del virus entre apiarios y regiones (Posada-Florez et al., 2019; Amiri et al., 2016; Wilfert et al., 2016). Además, se ha detectado la presencia ambiental del virus en flores, polen y cera, lo que sugiere posibles reservorios externos que contribuyen a su circulación (Alger et al., 2019; Schauer et al., 2023).
Una vez instalada la infección en la colmena el DWV puede provocar deformidad en las alas de abejas adultas que se infectaron durante su fase pupal, momento en que Varroa destructor introduce grandes cantidades de virus al alimentarse. Estas abejas suelen emerger con alas atrofiadas o arrugadas, abdomen acortado y color más oscuro, incapaces de volar ni participar en las tareas de la colonia (Imagen 1). En consecuencia, se reduce el número de obreras funcionales, pérdida de capacidad de termorregulación y debilitamiento general de la colmena (Lanzi et al., 2006; Martin et al., 2012).

Sin embargo, los signos visibles son relativamente raros, numerosos estudios han demostrado la existencia de infecciones asintomáticas, en las que las abejas se observan “sanas” pero portan el virus en niveles bajos o moderados sin mostrar alteraciones externas (McMahon y col., 2016; Ryabov y col., 2019). Estas infecciones “silenciosas” pueden persistir en el tiempo, afectando funciones fisiológicas y comportamentales: reducción en la longevidad, alteración de la capacidad olfativa, problemas en el aprendizaje, desorientación durante el vuelo, reducción en la eficiencia de forrajeo, menor capacidad de termorregulación y cambios sutiles en el comportamiento de nodrizas dentro de la colmena, con el consecuente descuido de la cría. Además, las abejas aparentemente sanas son por tanto reservorios y diseminadoras del virus, manteniendo la infección activa dentro del apiario sin que el productor lo advierta.
La presentación o no de signos clínicos esta directamente relacionada con la carga viral (cantidad de virus por abeja), en general, cuando la carga supera un umbral crítico (del orden de 100 a 1000 millones de copias por individuo según mediciones por RT-qPCR), se manifiestan deformidades y mortalidad temprana. Por debajo de ese nivel, las abejas pueden parecer normales, pero presentan una fisiología comprometida que reduce su eficiencia y expectativa de vida. Este fenómeno explica por qué colonias aparentemente fuertes pueden colapsar repentinamente durante el invierno: la proporción de abejas infectadas subclínicamente es alta y su recambio poblacional no alcanza a sostener la actividad de la colonia (Highfield y col., 2009; de Miranda & Genersch, 2010).
Para complejizar aun mas el panorama, existen variantes del virus de las alas deformadas, denominadas DWV-A, DWV-B, DWV-C y DWV-D. Estas variantes se definen como diferentes versiones genéticas del virus (con diferencias en su genoma) que puede comportarse de forma distinta en cuanto a tasa de replicación o virulencia. En Argentina Brasesco y col., (2021) han detectado 2 variantes (DWV-A y DWV-B), que difieren en su comportamiento biológico y principalmente en su interacción con Varroa destructor. Diversos estudios (Ryabov y col., 2019; Posada-Florez y col., 2021) demostraron que DWV-B se replica en las abejas y en el ácaro, mientras que DWV-A tiende a replicarse en las abejas. Esta capacidad de multiplicarse en Varroa destructor convierte a DWV-B en un vector más competente, favorece la transmisión de grandes cargas virales a las pupas y abejas adultas durante la alimentación del ácaro. En consecuencia, las colonias infectadas por DWV-B suelen tener cargas virales más altos, lo que se traduce en mayor mortalidad invernal y síntomas clínicos más marcados, mientras que las infecciones por DWV-A pueden mantenerse en niveles subclínicos durante más tiempo. Así, la replicación diferencial en Varroa destructor explica por qué la composición de variantes en una colonia influye directamente en la carga viral promedio y, por ende, en la severidad de los signos visibles y en la velocidad con que la infección se propaga (Mordecai y col., 2016; Ryabov y col., 2019; Posada-Florez y col., 2021).
Virus de la cría ensacada
El virus de la cría ensacada (SBV) que infecta principalmente a las larvas de las abejas. La enfermedad conocida como sacbrood o “cría ensacada” fue descrita hace más de un siglo, pero el agente viral fue caracterizado y aislado por primera vez de forma clara en estudios clásicos de L. Bailey y col (1964); desde entonces SBV ha sido ampliamente documentado y es uno de los virus más antiguos conocidos en apicultura. Al igual que DWV en 2010 Reynaldi y col. realizaron la primera detección molecular de SBV en el país.
El virus de la cría ensacada (SBV) puede ingresar y propagarse en las colmenas por diferentes vías, la transmisión oral o social ocurre cuando las larvas y las abejas adultas ingieren alimento contaminado, ya sea jalea real, néctar o miel, o bien durante los intercambios de alimento y cuidado entre obreras (trofalaxia). También se ha comprobado la transmisión vertical, en la que una reina infectada puede transferir el virus a su descendencia a través de los huevos o del esperma durante la cópula. A nivel de manejo, el ser humano puede favorecer la propagación del virus mediante la movilización de material biológico contaminado, como cuadros, enjambres o reinas infectadas, que actúan como fuente de infección en colmenas previamente sanas, a lo que se suman los fenómenos naturales como la deriva de vuelo o el pillaje.
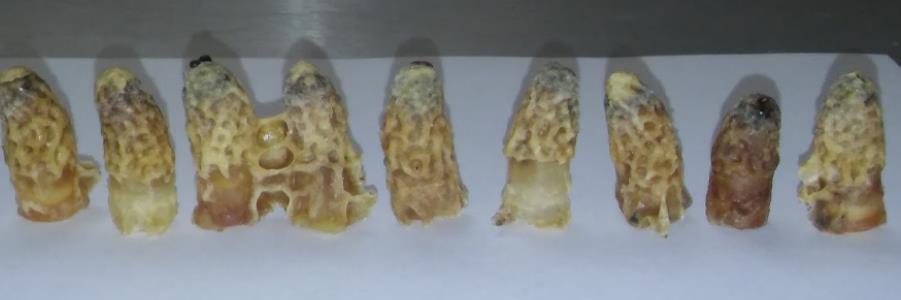
El virus de la cría ensacada (SBV) inicia su infección cuando las obreras nodrizas alimentan a las larvas con alimento contaminado, al consumir este alimento infectado, el virus ingresa al intestino medio de la larva, donde atraviesa las barreras epiteliales e inicia una replicación viral rápida y masiva. En pocos días, las partículas virales se diseminan a distintos tejidos, interfiriendo con el proceso normal de muda, la larva deja de secretar la enzima necesaria para desprender la cutícula vieja y queda atrapada dentro de un saco lleno de líquido, de ahí el nombre “cría ensacada” (Imagen 2).

A medida que la infección avanza, la larva cambia progresivamente de color blanco nacarado a amarillo pálido, luego grisáceo, y finalmente adopta una tonalidad marrón oscura o negra a medida que se seca, reflejo de la degradación de los tejidos, acumulación de partículas virales y líquidos corporales. El cuerpo de la larva pierde consistencia, se arruga y adquiere un aspecto escamoso que puede retirarse fácilmente del panal, a diferencia de otras enfermedades de la cría como la loque americana, donde la masa larval es pegajosa y difícil de extraer.
Tras la muerte de las larvas infectadas por el SBV, las abejas limpiadoras se infectan con el virus al manipulan y remover los restos larvales con alta carga viral. Aunque estas abejas adultas generalmente no manifiestan signos visibles de enfermedad, en ocasiones pueden experimentar una leve reducción en su longevidad y sufrir alteraciones en su comportamiento. No obstante, el mecanismo clave de perpetuación reside en que el virus SBV se replica activamente en las glándulas hipofaríngeas de las abejas infectadas. De este modo, luego de cumplir la función de limpiadores pasan a ocupar el rol de nodrizas, alimentando larvas con alimento que posee alta cargo de SBV, perpetuando el ciclo de infección dentro de la colmena.
El ácaro Varroa destructor también juega un papel complementario en este proceso. Aunque no se ha demostrado replicación activa de SBV en el acaro, sí actúa como vector mecánico y amplificador epidemiológico, ya que al alimentarse sobre las abejas provoca heridas que facilitan la entrada del virus y transporta partículas virales entre individuos. De este modo, Varroa destructor contribuye a aumentar la carga viral global de la colonia y favorece la aparición de brotes clínicos, especialmente cuando coincide con otros factores de estrés como desnutrición o alta densidad de cría.
Virus de la parálisis crónica de las abejas
El virus la parálisis crónica (CBPV) es un virus de distribución mundial asociado a cuadros de parálisis crónica en abejas melíferas. Aunque se conoce desde hace décadas, en los últimos años la detección y la incidencia lo han llegado a considerar una amenaza emergente en Europa. Dentro de la colonia, CBPV tiende a concentrarse en abejas adultas (particularmente las cargas virales son elevadas en cabeza y tejidos nerviosos). El ciclo” intra colmena” incluye transmisión directa entre obreras (tanto por contacto como por labores de limpieza) y contaminación del medio (cera, miel, superficies). Las abejas enfermas pueden permanecer en las colonias varios días antes de morir, excretando virus y elevando diseminación infecciosa local, lo que favorece contagios sucesivos y la aparición de focos en múltiples nidos del mismo apiario.
El virus de la parálisis crónica se manifiesta clínicamente en dos formas principales que, aunque distintas, pueden coexistir dentro de un mismo brote. La primera es la forma paralítica, caracterizada por abejas adultas que presentan temblores, dislocación de las alas, descoordinación motora e incapacidad para volar, permaneciendo agitadas en la piquera o en el piso de la colmena. En estos individuos suele observarse un abdomen distendido y pérdida progresiva de la capacidad de vuelo hasta que finalmente mueren (Budge y col., 2020; Ask IFAS, 2023). La segunda forma, conocida como “greasy” o de alopecia, se reconoce por la apariencia oscura y brillante del tegumento, debido a la pérdida de los pelos del cuerpo (Imagen 3). Estas abejas muestran un aspecto grasiento, diferente del brillo natural del exoesqueleto, y en etapas iniciales pueden volar, pero con el tiempo desarrollan debilidad, desorientación y caen cerca de la colmena. Además, estas abejas frecuentemente no son reconocidas como propias por la colonia, lo que lleva a las obreras a expulsarlas de la colmena, lo que se conoce como el “síndrome de los ladrones negros”.

 En muchos casos, ambas presentaciones de enfermedad se observan simultáneamente, reflejando distintos estadios de la infección o diferentes respuestas inmunológicas dentro de la misma colonia (Ribière y col., 2010; Dittes y col., 2020).
En muchos casos, ambas presentaciones de enfermedad se observan simultáneamente, reflejando distintos estadios de la infección o diferentes respuestas inmunológicas dentro de la misma colonia (Ribière y col., 2010; Dittes y col., 2020).
A diferencia de los virus que afectan principalmente a la cría, CBPV produce enfermedad principalmente en abejas adultas, especialmente en obreras. Las manifestaciones más severas se presentan con alteraciones neurológicas y cuticulares, ya que el virus afecta el tejido nervioso y las glándulas hipofaríngeas (Chen y col., 2014). Sin embargo, estudios moleculares recientes han detectado la presencia de material genético de CBPV en larvas y pupas, lo que sugiere que la infección puede extenderse a otras castas. La manifestación de enfermedad clásica, sin embargo, continúa siendo una patología de adultos, con impacto directo en la población obrera y, por ende, en la fuerza y productividad de la colonia.
En los individuos afectados, los signos clínicos más notorios son los temblores intensos, la descoordinación, la pérdida del vuelo y la tendencia a arrastrarse. Estas abejas a menudo se aglomeran cerca de la piquera o dentro del colmenar, mostrando alas desalineadas o dislocadas y movimientos espasmódicos que les impiden regresar al panal. En los casos de la forma “grasienta”, la cutícula brillante sin pilosidad da a los individuos un aspecto ennegrecido y reluciente, lo que facilita su reconocimiento durante las inspecciones sanitarias (Ask IFAS, 2023). A nivel de colonia, el CBPV provoca una pérdida continua de abejas adultas activas, lo que se traduce en debilitamiento general, reducción de la capacidad de pecoreo y eventual colapso si la mortalidad es elevada.
Virus del complejo AIK
El grupo de virus conocido como el Complejo de Parálisis Aguda de las Abejas comprende el Virus de la Parálisis Aguda (ABPV), el Virus de la Parálisis Aguda Israelí (IAPV) y el Virus de Cachemira (KBV). Se les considera un complejo debido a varias razones biológicas y epidemiológicas fundamentales: comparten una estructura viral y pertenecen a la misma familia filogenética (Dicistroviridae); tienen afinidad por los mismos tejidos de las abejas y en las manifestaciones de enfermedad, que incluyen temblores, desorientación, incapacidad para volar, parálisis progresiva y muerte fuera de la colmena (Imagen 5).
Además, estos virus con frecuencia se presentan en coinfecciones, un fenómeno que puede potenciar su mortalidad. Es crucial destacar que su impacto real sobre las colonias está altamente modulado por la presencia del ácaro Varroa destructor, que actúa como un co-factor amplificador de la replicación viral y facilita la aparición de brotes letales cuando las cargas víricas se elevan (de Miranda et al., 2010; Chen et al., 2014).
La vigilancia epidemiológica en el Latinoamerica ha confirmado la circulación de parte de este complejo viral. En Argentina, las primeras detecciones moleculares fueron realizadas por Reynaldi y colaboradores; en particular ABPV se identificó en 2010 (Reynaldi y col., 2010) y el IAPV fue reportado al año siguiente, en 2011 (Reynaldi y col., 2011). A la fecha el KBV no ha sido detectado en colonias argentinas. Sin embargo, su presencia en la región fue confirmada en el país vecino, ya que Riveros (2018) detectó el KBV en Chile, lo que subraya la importancia de la vigilancia regional para este patógeno.
Estos virus del complejo suelen provocar enfermedad principalmente en adultos, afectando la fisiología neuromuscular y comportamental de obreras y zánganos; no obstante, la detección molecular en larvas y en alimento larval demuestra que la cría puede ser expuesta oralmente y actuar como reservorio o víctima en determinadas condiciones, por lo que la etapa principal de expresión clínica sigue siendo la adulta, pero sin excluir la participación larval en la epidemiología (Yañez y col., 2020).
A nivel de colonia, la consecuencia inmediata de la infección por estos virus del complejo es una pérdida rápida de obreras funcionales: disminuye el número de forrajeadores activos, se rompe el ingreso de alimento y se reduce la capacidad de mantenimiento el nido de cría, decayendo la población de abejas y aumentando la mortalidad invernal (Molineri y col., 2017). El papel de Varroa destructor en esta ecuación es central y está sólidamente documentado: las infestaciones elevadas de Varroa están asociadas con incrementos drásticos en las cargas virales de pupas y adultos y con la conversión de infecciones latentes o subclínicas en brotes clínicos severos. En conjunto, la evidencia experimental, genómica y epidemiológica apoya que la sinergia entre alta carga viral de miembros del complejo (ABPV–IAPV–KBV) y elevada infestación por Varroa es uno de los factores más consistentes asociados a pérdidas de colmenas a escala regional y global.
Virus de las celdas reales negras
El Virus de las celdas reales negras (BQCV) afecta principalmente a las larvas de reina (Apis mellifera) durante su desarrollo en las celdas reales, provocando su muerte antes de la operculación o poco después. Las larvas infectadas se tornan de color amarillo, luego negras, dando el aspecto característico que da nombre al virus. En abejas adultas puede encontrarse de manera asintomática, pero su replicación se ve favorecida por condiciones de estrés y por la presencia de otros patógenos. Varroa puede actuar como vector mecánico y biológico, facilitando la diseminación del virus dentro de la colonia y aumentando la carga viral en las abejas parasitadas. La presencia de este virus en Argentina tiene una prevalencia baja, sin embargo paises vecinos, como Uruguay, reporta niveles de prevalencia en abejas adultas cercanos al 95%.
El control de BQCV se da principalmente e cabañas criadoras de abejas reinas donde, en primera instancia se trata de detectar la etapa donde se encuentra el virus presente. De esta manera, la forma de abordar esta infección viral es cambiando la colmena iniciadora. Si el problema continúa, se debe cambiar la colmena madre. Asimismo, el manejo integrado del colmenar es la mejor prevención ya que no existen tratamientos antivirales específicos. Es fundamental mantener colonias fuertes, bien alimentadas y con buena higiene. El control efectivo de Varroa destructor es una medida clave, pues la reducción del parasitismo limita la propagación del virus y mejora la resistencia inmunológica de las abejas. Además, se recomienda evitar el estrés por hacinamiento o manipulación excesiva, reemplazar panales viejos, y renovar reinas regularmente para mantener la vitalidad genética de la colonia. La selección de líneas de abejas con mayor resistencia natural a virus y ácaros también es una estrategia prometedora dentro de los programas de sanidad apícola.
Conclusión
Los virus que afectan a las abejas melíferas constituyen uno de los componentes más importantes del deterioro sanitario de las colmenas a nivel mundial. Aunque se han identificado más de una veintena de virus en Apis mellifera, solo algunos —como el virus de las alas deformadas (DWV), el virus de la parálisis crónica (CBPV) y los del complejo de parálisis aguda (ABPV, IAPV y KBV)— muestran relevancia clínica significativa. En la mayoría de los casos, estos patógenos se mantienen en forma subclínica, coexistiendo con la colonia sin provocar signos visibles ni mortalidad aparente. Este equilibrio se mantiene mientras las abejas conserven una buena condición inmunológica, nutricional y ambiental. Sin embargo, cuando factores de estrés externos —como déficit alimentario, exposición a pesticidas o condiciones climáticas adversas— alteran la homeostasis de la colonia, las infecciones virales pueden reactivarse, replicarse masivamente y traducirse en manifestaciones clínicas, pérdidas de cría o muerte de adultos, comprometiendo la supervivencia del enjambre.
En este escenario, el papel de Varroa destructor ha resultado determinante en el cambio de la dinámica viral en las abejas. Antes de su expansión global, muchos de estos virus circulaban de manera silenciosa, con baja carga y sin consecuencias evidentes. Sin embargo, la llegada del ácaro transformó radicalmente este escenario: su acción como vector biológico y amplificador mecánico de virus aumentó las tasas de transmisión y multiplicó las cargas virales dentro de las colmenas. La alimentación de Varroa sobre pupas y adultos provoca microlesiones en los tegumentos y hemolinfa, facilitando la entrada directa de partículas virales, y además genera inmunosupresión en las abejas, reduciendo su capacidad de respuesta antiviral. Así, infecciones que antes eran benignas o controladas, como las causadas por DWV o ABPV, se volvieron altamente patogénicas en presencia del ácaro, generando un verdadero cambio ecológico y epidemiológico en la salud apícola global.
Si bien actualmente, no existen tratamientos antivirales específicos para los virus de las abejas. Las estrategias de manejo se centran en controlar las poblaciones de Varroa destructor y en mantener colmenas fuertes, equilibradas y nutricionalmente adecuadas. La reducción de la carga del ácaro mediante rotación de principios activos, bioacaricidas o métodos biotécnicos, junto con el reemplazo periódico de reinas y la selección genética de colonias con mayor tolerancia, han demostrado disminuir la carga viral y la frecuencia de brotes clínicos. Además, el mantenimiento de un ambiente libre de estrés, la disponibilidad de recursos florales diversos y el monitoreo constante del estado sanitario permiten sostener una respuesta inmunológica activa en las abejas, minimizando la replicación viral y estabilizando el sistema de la colonia frente a agentes oportunistas.
Estas características de las infecciones virales requieren que el abordaje de esta problemática requiere una visión integral: mantener colmenas vigorosas, controlar de manera efectiva el ácaro y evitar condiciones que comprometan la fisiología y la inmunidad de las abejas. Solo así puede reducirse el peso de las infecciones virales y prevenir los colapsos que amenazan la estabilidad y productividad de los apiarios en todo el mundo.
Bibliografia.
Ask IFAS. (2023). Chronic Bee Paralysis Virus. University of Florida, Institute of Food and Agricultural Sciences.
Budge, G. E., De Miranda, J. R., Kinnersley, M., Rosser, N., & Jones, I. M. (2020). Chronic bee paralysis as a serious emerging threat to honey bee health. Nature Communications, 11(1), 2164.
Chen, Y. P., Siede, R., Evans, J. D., Li, J., & Pettis, J. S. (2014). Honey bee viruses and their effects on bee health. Current Opinion in Insect Science, 10, 97–104.
De Landa, G. F., De Donato, M., Landa, I. S., & Aldana, M. (2020). Detection of chronic bee paralysis virus (CBPV) in South American hymenopterans. Journal of Invertebrate Pathology, 174, 107474.
Dittes, J., Natsopoulou, M. E., Hülsmann, M., Hentschel, A., Moritz, R. F. A., & Becher, P. G. (2020). Overt Infection with Chronic Bee Paralysis Virus (CBPV) in Honey Bees. Viruses, 12(9), 970.
Ribière, M., Lallemand, P., & Schurr, F. (2010). Chronic bee paralysis: A disease and a virus like no other? Rev. Sci. Tech. Off. Int. Epiz., 29(2), 251–267.
Šimenc Kramar, N., Gombač, M., Poljak, M., Zorman, J., & Božič, J. (2024). Genomic diversity and transmission of Chronic Bee Paralysis Virus in European honey bee populations. Virology Journal, 21(1), 82.
Chen, Y. P., Higgins, Z., & DeGrandi-Hoffman, G. (2014). Honey bee viruses. In Viruses of Microorganisms (pp. 317-331). CRC Press.
de Miranda, J. R., Bailey, L., Ball, B. V., Blanchard, P., & Ryabov, E. V. (2010). Standard methods for virus research in Apis mellifera. Journal of Apicultural Research, 49(1), 49-60.
Reynaldi, F. J., Salina, M. D., Pecoraro, M., & Galosi, C. M. (2010). Molecular detection of Acute Bee Paralysis Virus (ABPV) in Argentinean honeybees (Apis mellifera). Veterinary Microbiology, 144(3-4), 481-484.
Reynaldi, F. J., Salina, M. D., García, M. L. G., & Galosi, C. M. (2011). First detection of Israeli Acute Paralysis Virus (IAPV) in Argentinean honeybees (Apis mellifera). Journal of Invertebrate Pathology, 107(1), 78-80.
Riveros, V. J. (2018). Detección molecular y prevalencia de virus en abejas melíferas (Apis mellifera L.) en la Región Metropolitana de Chile. (Tesis de Maestría, Universidad de Chile).
Yañez, O., et al. (2020). Routes of infection of bee viruses in Hymenoptera. Front Microbiol.
Molineri, A.I., et al. (2017). Prevalence of honey bee viruses in different regions of Argentina. (estudio regional).








